Le molteplici influenze del microbiota intestinale sulla salute e nei confronti di diverse patologie sono note da tempo, ma la relazione tra l’attività dei batteri e la fisiologia dell’ospite è ancora poco esplorata.
Due studi indipendenti, pubblicati sulla rivista Cell, descrivono un nuovo metodo per localizzare con precisione molteplici ceppi batterici e per controllarne l’attività.
I recenti progressi nelle tecniche di sequenziamento hanno permesso una caratterizzazione precisa delle specie batteriche che vivono nell’intestino, ma finora sono mancati gli strumenti per manipolare il microbioma. Ne sono stati sviluppati alcuni relativi per esempio all’Escherichia coli, ma questi strumenti non sono utili sui più comuni batteri appartenenti al genere bacteroides.
Nel primo studio, coordinato da Justin Sonnenburg presso la Stanford University School of Medicine – Stanford (USA), è descritto un metodo per manipolare geneticamente i bacteroides. Ciò consente di seguirne gli spostamenti nell’intestino attraverso alcuni promotori sintetici, sequenze di DNA che avviano la trascrizione di specifici geni.
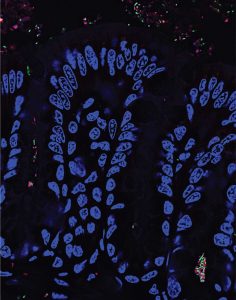
Attraverso questi promotori, il team di Sonnenburg ha stimolato in sei differenti specie di bacteroides la produzione di proteine fluorescenti di diverso colore, rosso o verde. Introdotte in roditori cresciuti in ambiente sterile, dopo due settimane le specie sono state osservate attraverso microscopi a fluorescenza su specifiche sezioni di tessuto del colon.
Sonnenburg e colleghi hanno poi condotto un esperimento separato, nel quale due differenti ceppi di bacteroides sono stati introdotti a distanza di una settimana l’uno dall’altro.
I ricercatori hanno potuto così osservare che il primo ceppo, una volta insediatosi nel colon, ha impedito la colonizzazione da parte del secondo. Un dato, questo, che conferma il ruolo dei batteri commensali nel respingere altre specie che possono invadere dall’esterno.
In futuro, il team intende sviluppare questi strumenti per spingere i batteri a produrre proteine in un momento o luogo specifico: «Questi strumenti possono permetterci di “somministrare” proteine a scopo terapeutico facendole produrre ai batteri che vivono nel nostro organismo» ha dichiarato Weston Whitaker, uno dei coordinatori dello studio. «L’uso di batteri per controllare il rilascio dei farmaci apre la porta a trattamenti intelligenti, che agiscono nel luogo giusto e nel momento giusto».
Il secondo studio è stato condotto alla Yale University School of Medicine – New Haven (USA) da un team di ricercatori guidato da Andrew Goodman. Anche in questo caso, sono stati sviluppati promotori sintetici in grado di controllare l’attività genica dei bacteroides. I ricercatori hanno introdotto specifici promotori nel genoma dei batteri e ne hanno controllato l’attività genica attraverso un sistema mediato dalla tetraciclina.
La presenza di un composto sintetico chiamato anidrotetraciclina permette ai batteri di attivare la trascrizione genica: senza il composto, l’attività dei geni è fermata del tutto. Il sistema funziona anche in vivo: l’aggiunta di differenti quantità di anidrotetraciclina nell’acqua ha permesso infatti di modulare l’attività genica su topi di laboratorio.
Applicato sugli esseri umani, l’approccio potrebbe permettere il rilascio “a comando” di composti a scopo terapeutico. L’anidrotetraciclina, che consente il controllo accurato dell’attività genica batterica su specifiche zone del tratto gastrointestinale, può essere poi somministrata con metodi differenti: attraverso cateterismo chirurgico oppure capsule a rilascio controllato.
Goodman e colleghi intendono applicare il sistema ad altri ceppi batterici e testarlo su altri tipi di interazione fra microbioma intestinale e organismo.
«Questi strumenti aprono la porta a nuovi tipi di studi per la comprensione del nostro microbioma e per definire in che modo i batteri commensali possono essere manipolati a scopo terapeutico» ha affermato Sonnenburg.
Prima che questo sia fattibile, tuttavia, saranno necessari altri studi che puntino a sviluppare metodi per colonizzare l’intestino umano in modo sicuro e affidabile.