L’uso di un probiotico multispecie mirato rappresenta una strategia efficace per la prevenzione della diarrea associata ad antibiotici (AAD), il controllo delle infezioni correlate e il mantenimento della salute intestinale e sistemica negli adulti anziani.1–7 La selezione specifica di formulazioni multispecie di alta qualità, scientificamente validate e comprovata capacità di colonizzazione, è essenziale per ottenere benefici clinicamente significativi.
Stato dell’arte
Con l’invecchiamento, il microbiota intestinale subisce cambiamenti profondi: in particolare, diminuiscono batteri benefici come Bifidobacterium e Lactobacillus, fondamentali per la salute intestinale e il benessere generale, non solo perché producono acidi grassi a catena corta (SCFA), ma anche per i loro molteplici ruoli nella barriera intestinale, nella modulazione immunitaria e nel controllo dei patogeni. Questi fenomeni favoriscono, quindi, disbiosi, infiammazione cronica di basso grado (il cosiddetto inflammaging), calo delle difese immunitarie e maggiore vulnerabilità a infezioni e complicanze metaboliche e neurodegenerative. 8,9 L’assunzione di farmaci come gli antibiotici contribuisce ulteriormente a questa disbiosi: fino al 10% degli anziani ospiti di case di riposo o ricoverati in ospedale assume antibiotici per infezioni comuni, aumentando il rischio di diarrea associata agli antibiotici (AAD, fino al 25%) 1,4 e di infezioni da Clostridioides difficile. 1,2,10
Probiotici e terapia antibiotica: i meccanismi chiave
Strategie mirate al ripristino dell’equilibrio del microbiota intestinale negli anziani includono l’impiego di probiotici multispecie, prebiotici e trapianto di microbiota fecale (FMT). I probiotici multispecie, oltre a essere sicuri e adatti alla somministrazione in questa popolazione, non solo riducono la diarrea associata agli antibiotici, ma agiscono a più livelli:
- ripristino dell’omeostasi intestinale: riequilibrano la comunità microbica e inibiscono patogeni.
- riduzione dell’infiammazione: stimolano la produzione di SCFA, modulano le citochine pro-infiammatorie e migliorano la secrezione di GLP-1 (glucagon-like peptide 1). 5
- rafforzamento della barriera intestinale: aumentano le proteine di giunzione stretta (occludina, claudine, ZO-1) e favoriscono la rigenerazione epiteliale.
- inibizione dei patogeni intestinali: controllo di Clostridioides difficile e altri batteri nocivi. 4,6,11
Cosa emerge dalle evidenze scientifiche
Una recente metanalisi Cochrane (2025) 12 basata su oltre 13 000 partecipanti ha mostrato che la co-somministrazione di probiotici può ridurre di circa il 50 % il rischio di Clostridioides difficile infection (CDI) nei pazienti trattati con antibiotici, suggerendo un beneficio clinico significativo nella prevenzione di CDI oltre alla diarrea associata agli antibiotici. Numerose evidenze cliniche indicano che l’assunzione del probiotico multispecie di indicazione specifica (Lactobacillus acidophilus W55, Lactobacillus acidophilus W37, Lactobacillus plantarum W1, Bifidobacterium lactis W51, Enterococcus faecium W54, Lactobacillus paracasei W20, Lactobacillus rhamnosus W71, Lactobacillus salivarius W24, Lactobacillus plantarum W62, Bifidobacterium bifidum W23) può contribuire in modo significativo nella prevenzione delle complicanze gastrointestinali associate alla terapia antibiotica. 4,7,13
Lo studio di Koning et al. (2008)7 ha valutato l’efficacia della somministrazione di un probiotico multispecie nella prevenzione della diarrea in soggetti sani trattati con amoxicillina. I risultati principali hanno mostrato che l’incidenza di diarrea era significativamente più bassa nel gruppo trattato con il probiotico (48%), rispetto al gruppo placebo (79%), accompagnata da una riduzione significativa dei movimenti intestinali diarroici e da un miglioramento della consistenza delle feci, valutata tramite la Bristol Stool Form Scale (Fig. 1a). Inoltre, l’assunzione del probiotico ha determinato una colonizzazione temporanea da parte di ceppi di Enterococcus presenti nella formulazione, contribuendo a stabilizzare transitoriamente la comunità microbica intestinale durante il trattamento antibiotico (Fig. 1b).7
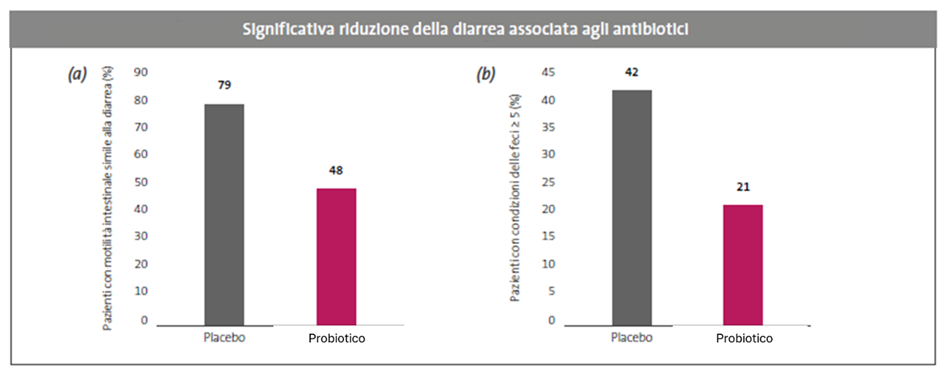
Figura 1: (a) Durante il periodo di osservazione di 2 settimane, i partecipanti del gruppo probiotico hanno mostrato un’incidenza significativamente più bassa di evacuazioni diarroiche (p < 0,05). (b) Il numero di soggetti che hanno sofferto di diarrea—definito come consistenza delle feci ≥ tipo 5 sulla scala di Bristol, per almeno 2 giorni consecutivi — è stato significativamente ridotto nel gruppo che ha assunto il probiotico (p < 0,05).7
Lo studio di Van Wietmarschen et al. (2020)4 ha valutato l’effetto dell’assunzione di un probiotico multispecie (Lactobacillus acidophilus W55, Lactobacillus acidophilus W37, Lactobacillus plantarum W1, Bifidobacterium lactis W51, Enterococcus faecium W54, Lactobacillus paracasei W20, Lactobacillus rhamnosus W71, Lactobacillus salivarius W24, Lactobacillus plantarum W62, Bifidobacterium bifidum W23) nella prevenzione della diarrea associata ad antibiotici (AAD) in residenti anziani, condotto durante le attività quotidiane nelle case di riposo. Durante 167 episodi di trattamento antibiotico, l’integrazione con il probiotico è stata associata a una riduzione significativa dell’incidenza di AAD, rispetto agli episodi senza probiotico (20 % vs 36 %, p = 0,022, Fig. 2), evidenziando l’efficacia del probiotico nel ridurre un rischio clinicamente rilevante in una popolazione così vulnerabile. 4
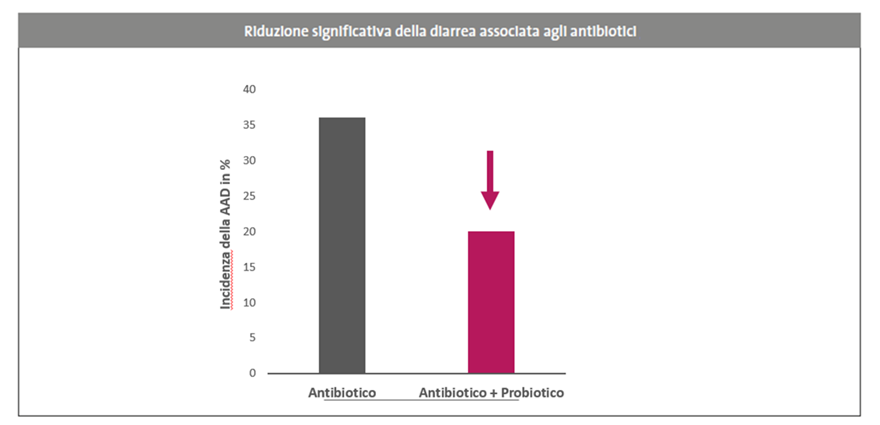
Figura 2: La somministrazione di un probiotico multispecie ha ridotto l’incidenza di AAD in modo significativo nei pazienti ricoverati in una casa di riposo per anziani.4
Lo studio pilota condotto da Zollner-Schwetz et al.(2020)13ha valutato l’effetto dell’assunzione di un probiotico multispecie in pazienti di una struttura di lunga degenza colonizzati da batteri Gram-negativi multi-resistenti (MRGN). Dopo 12 settimane di integrazione, la colonizzazione intestinale da MRGN si è ridotta in modo significativo, con un effetto protettivo ancora rilevabile (-58%) nelle 12 settimane successive alla sospensione del probiotico (Fig. 3a). L’analisi del microbioma cutaneo ha mostrato una riduzione ancora più marcata della colonizzazione inguinale (-71%, Fig. 3b) durante la somministrazione, sebbene il beneficio sia diminuito dopo l’interruzione del trattamento. Questi risultati suggeriscono che la modulazione della risposta immunitaria tramite l’asse intestino-pelle è più efficace durante la somministrazione continua del probiotico, confermando il suo potenziale ruolo come strategia di supporto nel controllo delle infezioni da batteri multi-resistenti, in popolazioni fragili e ospedalizzate. Inoltre, lo studio mostra che l’integrazione con un probiotico multispecie esercita effetti mirati su specifici gruppi batterici, con un aumento relativo di Enterococcus e di membri della famiglia Ruminococcaceae nell’intestino, e una modulazione di Actinotignum e Aerococcus sulla cute, coerenti con una colonizzazione transitoria ma funzionalmente significativa. 13
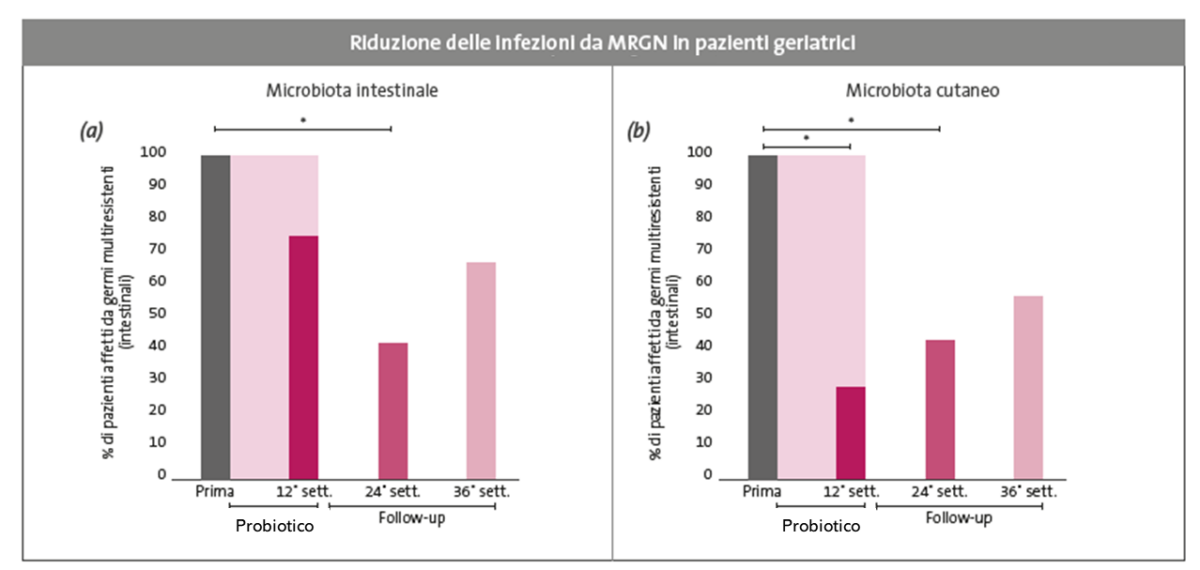
Figura 3: (a) L’integrazione probiotica ha portato a una riduzione costante delle infezioni intestinali causate da batteri multi-resistenti durante il periodo di trattamento di 12 settimane. (b) L’analisi del microbiota cutaneo ha mostrato una diminuzione del 71% della colonizzazione batterica multi-resistente durante la somministrazione di probiotici.13
In pazienti con infezione da COVID‑19 in forma lieve, lo studio di Horvath et al. (2024) 14 ha valutato l’effetto della somministrazione di un probiotico multispecie sul microbiota intestinale e sui sintomi gastrointestinali. Il trattamento probiotico ha contribuito a modulare significativamente la composizione microbica, aumentando la diversità beta del microbiota e favorendo l’introduzione di Enterococcus faecium W54, rispetto al placebo. Sebbene i sintomi gastrointestinali e respiratori siano migliorati nel tempo in entrambi i gruppi, lo studio suggerisce che la terapia probiotica può ripristinare la diversità microbica e supportare l’equilibrio intestinale.14
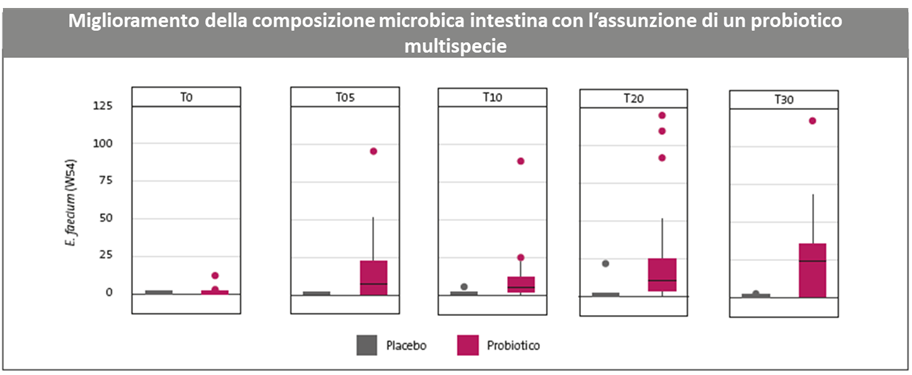
Figura 4: La somministrazione giornaliera del probiotico multispecie con indicazione medica specifica per 30 giorni ha portato a un aumento sostenuto di Enterococcus faecium.14
L’impatto dei risultati
Interventi mirati sul microbiota, come l’integrazione con probiotici multispecie e di rilevanza clinica, si sono dimostrati strumenti efficaci per contrastare la disbiosi legata all’invecchiamento, nonché ridurre la vulnerabilità alle infezioni e agli effetti collaterali della terapia antibiotica. La somministrazione di ceppi probiotici multispecie di indicazione specifica e rilevanza medica aiuta a prevenire la diarrea associata ad antibiotici (AAD) e a limitare il rischio di infezioni da Clostridioides difficile,2,4–7,10 preservando la diversità microbica, rafforzando la resistenza alla colonizzazione e modulando le risposte immunitarie.
Conclusioni
L’evidenza scientifica attuale conferma che l’assunzione di probiotici multispecie rappresenta uno strumento efficace per la prevenzione della diarrea da antibiotici, il controllo delle infezioni correlate e il mantenimento della salute intestinale e sistemica negli anziani.1,2,4–7 La selezione di formulazioni ad alta qualità, con capacità di colonizzazione comprovata, è fondamentale per ottenere benefici clinici significativi.
Bibliografia
1. Stadlbauer, V. et al. Dysbiosis in early sepsis can be modulated by a multispecies probiotic: a randomised controlled pilot trial. Benef. Microbes 10, 265–278 (2019).
2. Hood, K. et al. Probiotics for Antibiotic-Associated Diarrhoea (PAAD): a prospective observational study of antibiotic-associated diarrhoea (including Clostridium difficile-associated diarrhoea) in care homes. Health Technol. Assess. (Rockv). 18, 1–84 (2014).
3. Shen, N. T. et al. Timely Use of Probiotics in Hospitalized Adults Prevents Clostridium difficile Infection: A Systematic Review With Meta-Regression Analysis. Gastroenterology 152, 1889-1900.e9 (2017).
4. Van Wietmarschen, H. A., Busch, M., Van Oostveen, A., Pot, G. & Jong, M. C. Probiotics use for antibiotic-associated diarrhea: a pragmatic participatory evaluation in nursing homes. BMC Gastroenterology 2020 20:1 20, 151- (2020).
5. Yang, S. et al. Prevention and treatment of antibiotics-associated adverse effects through the use of probiotics: A review. J. Adv. Res. 71, 209–226 (2025).
6. Hell, M. et al. Probiotics in Clostridium difficile infection: reviewing the need for a multistrain probiotic. Benef. Microbes 4, 39–51 (2013).
7. Koning, C. J. M. et al. The effect of a multispecies probiotic on the intestinal microbiota and bowel movements in healthy volunteers taking the antibiotic amoxycillin. Am. J. Gastroenterol. 103, 178–189 (2008).
8. N V, K. & M, S. Aging through the lens of the gut microbiome: Challenges and therapeutic opportunities. Archives of Gerontology and Geriatrics Plus 2, 100142 (2025).
9. Gyriki, D. et al. The gut microbiota and aging: interactions, implications, and interventions. Frontiers in Aging 6, 1452917 (2025).
10. Smits, W. K., Lyras, D., Lacy, D. B., Wilcox, M. H. & Kuijper, E. J. Clostridium difficile infection. Nat. Rev. Dis. Primers 2, 1–20 (2016).
11. Mercado-Monroy, J., Falfán-Cortés, R. N., Muñóz-Pérez, V. M., Gómez-Aldapa, C. A. & Castro-Rosas, J. Probiotics as modulators of intestinal barrier integrity and immune homeostasis: a comprehensive review. J. Sci. Food Agric. https://doi.org/10.1002/jsfa.70168 (2025) doi:10.1002/jsfa.70168.
12. Probiotics for the prevention of Clostridioides difficile‐associated diarrhea in adults and children – Esmaeilinezhad, Z – 2025 | Cochrane Library. https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD006095.pub5/full.
13. Zollner-Schwetz, I. et al. Effect of a Multispecies Probiotic on Intestinal and Skin Colonization by Multidrug-Resistant Gram-Negative Bacteria in Patients in a Long-Term Care Facility: A Pilot Study. Nutrients 12, (2020).
14. Horvath, A. et al. Probiotic Therapy of Gastrointestinal Symptoms During COVID-19 Infection: A Randomized, Double-Blind, Placebo-Controlled, Remote Study. Nutrients 2024, Vol. 16, 16, (2024).











