Le malattie metaboliche come obesità, diabete di tipo 2 e sindrome metabolica sono sempre più diffuse e rappresentano un rischio significativo per la salute epatica.
Queste condizioni possono compromettere la funzione del fegato, spesso in modo asintomatico nelle fasi iniziali, complicando il trattamento e ritardando la diagnosi. Proteggere il fegato in una fase precoce è quindi cruciale per prevenire complicanze future.
I probiotici, grazie alla loro capacità di modulare positivamente il microbioma intestinale, stanno emergendo come un’opzione promettente per il miglioramento della salute epatica e la prevenzione delle patologie croniche del fegato.
Il ruolo chiave dell’asse intestino-fegato
L’asse intestino-fegato rappresenta una connessione diretta tra l’intestino e il fegato tramite la vena porta, la quale trasporta metaboliti prodotti dai microbi intestinali direttamente al fegato [1].
Recenti studi hanno dimostrato che la disbiosi intestinale, ossia uno squilibrio nel microbioma, può influire negativamente sul fegato, favorendo lo sviluppo di malattie epatiche croniche come la malattia del fegato grasso non alcolica (NAFLD) e la sua forma più avanzata, la steatoepatite non alcolica (NASH) [2].
Ad esempio, sia in modelli animali che nell’uomo, è stato osservato che l’infiammazione del colon aumenta la permeabilità intestinale in casi di cirrosi o NASH, facilitando il passaggio di batteri e dei loro prodotti verso il fegato [3]. La disbiosi, quindi, non solo incrementa la permeabilità intestinale, ma provoca anche infiammazione nella parete intestinale, il cosiddetto “leaky gut” [4-6], favorendo la traslocazione di endotossine nel sangue, un processo che peggiora l’infiammazione e accelera il deterioramento del tessuto epatico [7].
NAFLD e NASH: la crescente prevalenza delle malattie epatiche croniche
Le malattie croniche del fegato, in particolare la NAFLD, rappresentano una delle cause più comuni di morte a livello mondiale, con una prevalenza globale stimata intorno al 25%.
La progressione da NAFLD a NASH è caratterizzata dall’accumulo di grasso negli epatociti, accompagnato da infiammazione e fibrosi. Se non trattate, queste condizioni possono evolvere in cirrosi epatica e, nei casi più gravi, in carcinoma epatocellulare.
La cirrosi rappresenta lo stadio finale delle malattie epatiche croniche, durante il quale il fegato perde la sua capacità di detossificare l’organismo, portando a un aumento delle tossine nel sangue (endotossinemia) e a un indebolimento del sistema immunitario [8].
Probiotici e salute epatica: nuove evidenze scientifiche
Il potenziale ruolo dei probiotici multispecie nel miglioramento della funzione epatica è sempre più oggetto di studio. Grazie alla loro capacità di ristabilire l’equilibrio del microbiota intestinale, i probiotici possono contribuire a ridurre l’infiammazione sistemica, rafforzando la barriera intestinale e riducendo il rischio di ulteriori danni epatici [9-11].
Uno studio randomizzato, in doppio cieco e controllato con placebo condotto presso l’Università Medica di Graz ha evidenziato che un probiotico multispecie composto da ceppi batterici selezionati (Bifidobacterium bifidum W23, Bifidobacterium lactis W52, Lactobacillus acidophilus W37, Lactobacillus brevis W63, Lactobacillus casei W56, Lactobacillus salivarius W24, Lactococcus lactis W19 and Lactococcus lactis W58) ha migliorato significativamente le funzioni epatiche e immunitarie in pazienti con cirrosi epatica compensata (punteggio Child Pugh <12) [12], riducendo la permeabilità intestinale e favorendo il ripristino della barriera intestinale (punteggi Child-Pugh e MELD) rispetto al gruppo placebo (Fig. 1).
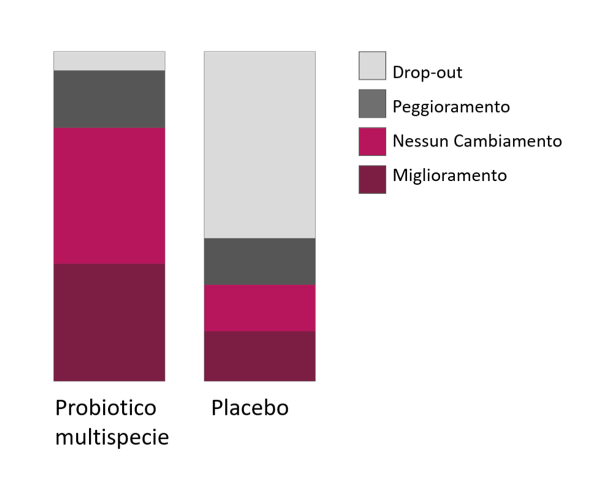
Fig. 1 La somministrazione di un probiotico multispecie per sei mesi porta a un notevole miglioramento di tutte le funzioni epatiche (punteggio Child-Pugh) nei pazienti con cirrosi epatica.
In un altro studio, è stato dimostrato nella stessa coorte di pazienti che l’uso di questo probiotico ha portato a un cambiamento positivo del microbiota intestinale [13]. L’aumento della popolazione di batteri benefici come Faecalibacterium prausnitzii e la riduzione dei marker di infiammazione intestinale (Fig. 2) hanno evidenziato il ruolo cruciale del microbiota intestinale nel modulare la risposta epatica.

Fig. 2 a) L’assunzione di un probiotico multispecie per sei mesi porta a un significativo aumento dei ceppi batterici capaci di formare SCFA essenziali. b) L’aumentata abbondanza di Prevotella sp. e Syntrophococcus sucromutans è correlata a un miglioramento significativo della barriera intestinale.
Effetti dei probiotici su altre malattie metaboliche correlate
La stessa combinazione di ceppi probiotici specifici ha mostrato effetti benefici anche sulle condizioni metaboliche legate al diabete di tipo 2 (T2DM) e all’obesità, due dei principali fattori di rischio per lo sviluppo della NAFLD. È già noto come il microbiota intestinale giochi un ruolo cruciale nello sviluppo di condizioni correlate, come la resistenza all’insulina nel T2DM [14], nella riduzione della produzione di acidi grassi a catena corta (SCFA), e nell’influenza negativa di metaboliti batterici, come la flagellina, l’acido lipoteicoico e il peptidoglicano, sulle giunzioni strette tra le cellule epiteliali intestinali. Questi metaboliti attivano i segnali TRL2 e TRL4, contribuendo all’infiammazione [15].
L’integrazione con probiotici è stata associata a una riduzione dei marker di infiammazione sistemica e a un miglioramento dell’integrità della barriera intestinale. In pazienti con diabete di tipo 2 e obesità, è stato osservato un miglioramento di qualità della vita e una riduzione della circonferenza addominale [16], indicando che la modulazione del microbiota intestinale può avere effetti positivi sia sulla salute epatica che su quella metabolica.
L’uso combinato di un probiotico multispecie specifico e di un prebiotico a base di glucomannano di konjac, che stimola la proliferazione dei produttori di SCFA, ha ulteriormente migliorato sia l’integrità della barriera intestinale sia la qualità di vita dei pazienti (Fig. 3).

Fig. 3 La somministrazione per tre mesi di un probiotico multispecie in combinazione con un prebiotico rafforza la barriera intestinale e migliora la qualità di vita. a) Riduzione significativa della permeabilità intestinale (“Leaky-Gut”). b) Miglioramento significativo dell’attività fisica.
Prospettive future: una strategia preventiva e terapeutica promettente
Alla luce delle nuove scoperte scientifiche, i probiotici multispecie stanno emergendo come una strategia preventiva e terapeutica efficace per le malattie epatiche croniche. La loro capacità di ripristinare l’equilibrio del microbioma intestinale e di conseguenza ridurre l’infiammazione rende i probiotici un’opzione interessante non solo per i pazienti con patologie epatiche in fase iniziale, ma anche per chi è a rischio di sviluppare malattie metaboliche del fegato.
Con l’aumento delle malattie epatiche croniche a livello globale, è cruciale considerare interventi preventivi basati sull’evidenza scientifica. Il futuro della gestione delle malattie del fegato potrebbe risiedere nell’adozione di probiotici come complemento ai trattamenti tradizionali, aprendo la strada a un approccio integrato alla salute intestinale ed epatica.
Contenuto realizzato con la sponsorizzazione non condizionante dell’Istituto AllergoSan.
Reference
[1] Tripathi, A. et al. The gut-liver axis and the intersection with the microbiome. Nat Rev Gastroenterol Hepatol 15, 397 (2018).
[2] Younossi, Z. M. Non-alcoholic fatty liver disease – A global public health perspective. J Hepatol 70, 531–544 (2019).
[3] Imai J. et al., The pathogenic oral–gut–liver axis: new understandings and clinical implications.
Expert Rev Clin Immunol. 2021;17:727–736.
[4] Safari, Z. & Gérard, P. The links between the gut microbiome and non-alcoholic fatty liver disease (NAFLD). Cellular and Molecular Life Sciences 2019 76:8 76, 1541–1558 (2019).
[5] Qin, N. et al. Alterations of the human gut microbiome in liver cirrhosis. Nature 513, 59–64 (2014).
[6] Bajaj, J. S. et al. Altered profile of human gut microbiome is associated with cirrhosis and its complications. J Hepatol 60, 940–947 (2014).
[7] Albillos, A., de Gottardi, A. & Rescigno, M. The gut-liver axis in liver disease: Pathophysiological basis for therapy. J Hepatol 72, 558–577 (2020).
[8] Leber, B., Mayrhauser, U., Rybczynski, M. & Stadlbauer, V. Innate immune dysfunction in acute and chronic liver disease. Wiener klinische Wochenschrift 2009 121:23 121, 732–744 (2009).
[9] Szabo, G. Gut-Liver Axis in Alcoholic Liver Disease. Gastroenterology 148, 30 (2015).
[10] Wiest, R., Albillos, A., Trauner, M., Bajaj, J. S. & Jalan, R. Targeting the gut-liver axis in liver disease. J Hepatol 67, 1084–1103 (2017).
[11] Brandl, K., Kumar, V. & Eckmann, L. Microbiome and Host Interactions: Gut-liver axis at the frontier of host-microbial interactions. Am J Physiol Gastrointest Liver Physiol 312, G413 (2017).
[12] Horvath, A. et al. Randomised clinical trial: the effects of a multispecies probiotic vs. placebo on innate immune function, bacterial translocation and gut permeability in patients with cirrhosis. Aliment Pharmacol Ther 44, 926–935 (2016).
[13] Horvath, A. et al. Changes in the Intestinal Microbiome during a Multispecies Probiotic Intervention in Compensated Cirrhosis. Nutrients 12, 1874 (2020).
[14] Gurung M. et al., Role of gut microbiota in type 2 diabetes pathophysiology. EBioMedicine
2020;51:102590
[15] Ebrahimzadeh Leylabadlo H. et al., From role of gut microbiota to microbial-based therapies
in type 2-diabetes. Infect. Genet. Evol. 2020; 81:104268
[16] Horvath, A. et al. Effects of a multispecies synbiotic on glucose metabolism, lipid marker, gut microbiome composition, gut permeability, and quality of life in diabesity: a randomized, double-blind, placebo-controlled pilot study. Eur J Nutr 59, 2969–2983 (2020).









