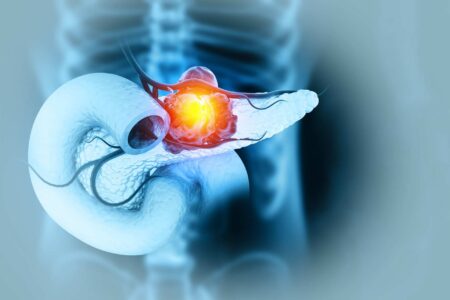
L’adenocarcinoma pancreatico (PAAD) viene considerato una malattia omogenea, e questo può contribuire alla mancanza di miglioramenti significativi nella prognosi del paziente rispetto ad altri tumori.
Le alterazioni molecolari e fisiologiche alla base di PAAD sono diverse e non completamente comprese. Di conseguenza, identificare possibili meccanismi di sviluppo del tumore, inclusa l’influenza del microbioma, rimane una sfida aperta.
Uno studio recente, i cui risultati sono stati pubblicati sulla rivista Carcinogenesis, ha indagato l’associazione tra un batterio, Porphyromonas gingivalis intratumorale e l’adenocarcinoma pancreatico.
Batteri e carcinogenesi
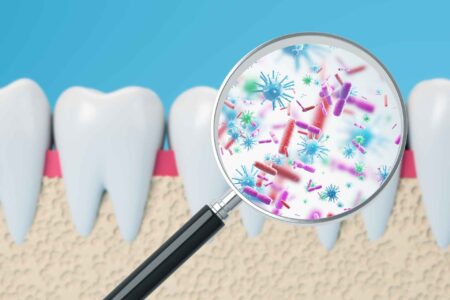
I microrganismi possono influire sugli esiti del cancro e influenzare il microambiente tumorale. Ad esempio, l’eradicazione di H. pylori riduce il rischio di cancro gastrico ed è spesso curativa nel linfoma del tessuto linfoide associato alla mucosa.
Studi compiuti sulle alterazioni del microbioma pancreatico hanno mostrato una forte associazione tra il cancro al pancreas e il batterio Porphyromonas gingivalis, un patogeno predominante nella malattia parodontale.
In alcune circostanze P. gingivalis può invadere le cellule ospiti e manipolare i meccanismi di segnalazione che distorcono la composizione del microambiente della popolazione di cellule immunitarie del microambiente che promuovono la sopravvivenza batterica e l’evasione immunitaria.
L’immunomodulazione di P. gingivalis determina l’up-regulation dei fattori microambientali associati all’infiammazione cronica, alla tolleranza alle mutazioni e all’interruzione delle normali funzioni apoptotiche, che sono tutti ben noti fattori di rischio per lo sviluppo del cancro.
Correlazione tra carcinoma pancreatico e P. gingivalis
La letteratura recente ha correlato P. gingivalis con il carcinoma pancreatico in vari modi, inclusi titoli plasmatici più elevati di anticorpi contro P. gingivalis nei pazienti affetti da carcinoma pancreatico, esposizione orale a P. gingivalis con sviluppo accelerato di carcinoma pancreatico in topi transgenici KRAS G12D, infezione da parte di P. gingivalis di tumori pancreatici xenotrapiantati con aumento delle dimensioni del tumore nei topi, infezione intracellulare di linee cellulari da parte di P. gingivalis con preregolazione di oncogeni e progressione del cancro in vari contesti.
Profilo molecolare del tumore al pancreas
L’eterogeneità molecolare di PAAD è un possibile fattore di confusione quando si tenta di correlare lo sviluppo del tumore con altri fattori biologici, inclusi componenti batterici specifici del microbioma, come P. gingivalis.
Per comprendere meglio la complessità e l’eterogeneo panorama oncogenico del carcinoma pancreatico, uno studio genomico multi-istituto ha suddiviso il carcinoma pancreatico in nove programmi genetici (GP1-9).
Questi nove programmi sono stati presi in considerazione per una correlazione più precisa dei batteri e uno specifico profilo molecolare e oncogenico, durante l’esplorazione della connessione tra P. gingivalis e PAAD. Si è visto che l’aumento dell’espressione dei geni che rappresentano il profilo del programma genico 7 (GP7) era altamente correlato con la positività di P. gingivalis.
P. gingivalis e macrofagi M2 in PAAD
Uno dei tratti distintivi del profilo GP7 è l’espressione dei marcatori dei macrofagi M2. È stato dimostrato che la polarizzazione dei macrofagi a un fenotipo M2 ha effetti immunosoppressivi e incentiva lo sviluppo tumorale con livelli aumentati di espressione di HAVCR2, CSFR1, PDL2 e MS4A4 come osservato in GP7.
È stato dimostrato che P. gingivalis promuove la polarizzazione dei macrofagi a M2, con livelli aumentati di antigeni associati a M2. GP7 è anche caratterizzato da alcuni marcatori di cellule T, ad esempio CD2, CD4, IL2RA, FOXP3, C3AR1, CD53, CTLA-4 e CD274, molti dei quali sono anche associati alla presenza di P. gingivalis.
Disregolazione dei marcatori del sistema immunitario
La sovraregolazione dei marcatori del sistema immunitario innato è un’altra caratteristica osservata sia nelle infezioni da P. ginigvalis che nei profili GP7. Infatti, sia nei microambienti di P. gingivalis che nel profilo GP7 si osservano sovraregolazione e modificazione delle proteine citoscheletriche.
Si ritiene che questa disregolazione citoscheletrica sia coinvolta nell’assorbimento cellulare di P. gingivalis, nella minimizzazione batterica dell’autofagia e nell’evasione batterica della clearance extracellulare. In sintesi, P. gingavalis potrebbe essere responsabile di GP7 in PAAD.
Si è evidenziata anche una correlazione tra le caratteristiche del recettore immunitario adattativo al tessuto PAAD positivo per P. gingivalis, a livello di recupero delle letture di ricombinazione IG dal tessuto PAAD. I recuperi di ricombinazione IG sono correlati con infiltrati di cellule B e sono stati associati a una ridotta sopravvivenza in PAAD.
Inoltre, le sequenze di amminoacidi TCR CDR3 nei campioni P. gingivalis-negativi hanno dimostrato una maggiore complementarità con le sequenze di amminoacidi note degli antigeni di P. gingivalis. Quest’ultimo risultato può essere coerente con la possibilità che una migliore risposta del TCR a P. gingivalis riduca il livello di P. gingivalis nel tessuto PAAD.
Conclusioni
Nel complesso, i dati dello studio rimangono coerenti con l’ipotesi secondo cui il controllo delle infezioni da P. gingivalis riduce al minimo lo sviluppo di PAAD.
Inoltre, i dati riportati possono essere utili per guidare le terapie e stabilire biomarcatori prognostici per le suddivisioni dei pazienti con PAAD.
Infine, va anche notato che, in alcuni casi, considerando la prospettiva Pan-Cancro, il microbioma può effettivamente ridurre l’incidenza dello sviluppo del cancro.